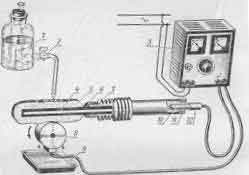
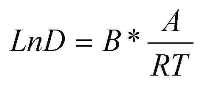 Первым выделение металлов под действием электрического тока из растворов солей изучил Б.С.Якоби, исследования которого положили начало гальваностегии.
Первым выделение металлов под действием электрического тока из растворов солей изучил Б.С.Якоби, исследования которого положили начало гальваностегии.
Процесс электрокристаллизации металлов обычно разделяют на три стадии:
1 Миграция разряжающихся ионов из электролита к поверхности электродов, то есть прохождение ионов через диффузный слой к наружней границе электрического двойного слоя;
2 Проход ионов со стороны электролита на границе фаз к металлу (стадия включает десольвацию (частичную) ионов металлов, прохождение их через электрический двойной слой и превращение их в адсорбированные ионы и атомы),
3 Диффузия к местам роста и создания кристаллической решетки адсорбированных ионов и образование двух и трехмерных зародышей.
Скорость всего электрохимического процесса определяется самой медленной стадией, сопровождающейся наибольшим торможением. Различают три вида поляризации: концентрационную, химическую (электрохимическую) и фазовую, которые служат основой для классификации электрохимических процессов. Тип поляризации может быть определен по абсолютной величине эффективной энергии, которая необходима чтобы катион металла восстанавливался на катоде. Эффективная энергия активации электрохимической реакции может быть определена при постоянном потенциале по линейной зависимости логарифма силы тока от обратного значения температуры (по уравнению Аррениуса):
где D- это плотность тока, а/см2;
В- константа;
- тангенс угла наклона к оси абцисс;
Т- температура.
Факторы, которые влияют на катодную поляризацию во время электроосаждения, должны соответствующим образом менять также и структуру получающихся осадков. К ним можно отнести: плотность тока, концентрацию ионов, а также их природу, состояние поверхности электродов, температуру электролитов, добавки различных веществ к электролиту.
Олово в растворах простых солей кристаллизуется в виде дендридов. При этом получается рыхлый и губчатый осадок, непригодный для практического использования. Получить мелкокристаллический осадок в электрохимии не удается даже путем изменения плотности тока, температуры и концентрации электролита. Однако, установлено, что олово осаждается в виде мелкокристаллического осадка в присутствии коллоидных и поверхностно –активных веществ. Изучение процесса осаждения олова в присутствии добавок показало значительное увеличение поляризации по сравнению с осаждением без добавления поверностно-активных веществ. При увеличении концентрации органических присадок к электролиту происходит снижение катодного выхода по току и уменьшение адсорбционной предельной плотности тока.
Исследование процесса осаждения олова в кислых электролитах показало, что кинетика процесса подчиняется теории адсорбционной химической поляризации. Это явление называют эффектом Лошкарева. Дальнейшими исследованиями установлено, что введение в электролит лужения добавок, образующих адсорбционные слои катионов, приводит к наибольшим значениям катодной поляризации. Установлено также, что эффективность добавок ионного типа намного выше, чем молекулярного. Большая поляризация при электроосаждении олова в присутствии органических веществ объясняется образованием на катоде плотных, почти непроникаемых для ионов адсорбционных слоев. На основании этого открытия разработано много различных электролитов для получения монокристаллических осадков олова. Однако, существенным недостатком этих электролитов является ограниченность диапазона плотностей тока, при которых получаются блестящие мелкокристаллические покрытия.
Исследования механизма процессов, происходящих при электроосаждении олова в присутствии органических добавок, позволили разработать линии электролитического лужения на основе фенолсульфоновой или серной кислоты, называемые часто линиями «Ферростан». В настоящее время непрерывные линии лужения значительно модернизированы, как в отношении механического и электрического оборудования, так и в отношении применяемой технологии.